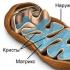
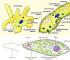
Test auf Alkane-Basisstufe. Test "Alkana"
Untersuchung in der Chemie von Alkanen mit Antworten für Studierende von 10. Die Prüfung besteht aus 3 Optionen in jeweils 6 Aufgaben.
1 Option
1. Strukturelle Formel von Alkan:
2. Isomer sind:
1) Bhutan und Pentan
2) 2-Methylbutan und 2,2-dimethylpropan
3) 1,3-Dimethylpentan und 2-methylpenan
4) 3,3-Dimethylpentan und 2,2-Dimethylbutan
3.
A. Mit einer Erhöhung des relativen Molekulargewichts in den Alkananen erhöhen Sie die schmelzenden und kochenden Temperaturen.
B. Methan hat einen charakteristischen Geruch.
1) ist nur wahr
2) True nur b
3) Beide Urteile sind wahr
4) Beide Urteile sind falsch
4. In der Gleichung der Verbrennungsreaktion ist der Pentankoeffizient vor der Sauerstoffformel:
1) 2
2) 4
3) 6
4) 8
5. Synthesegas ist als Ergebnis der Reaktion zwischen:
1) Methan und Sauerstoff
2) Methan und Chlor
3) Methan und Wasser
4) Chlormethan und Wasser
6. Berechnen Sie die Masse des Aluminiumcarbids Al 4 C3, das erforderlich ist, um 112 Liter (N.U.) von Methan zu erhalten, wenn der Volumenanteil der Reaktionsproduktausgabe 80% theoretisch möglich ist.
Option 2
1. Molekulare Formel von Alkan:
1) mit 4 h 10
2) C 3 H 4
3) c 6 h 6
4) c 5 h 10
2. Die gleiche Zusammensetzung und Eigenschaften der Substanz sind durch Strukturformeln dargestellt:

3. Propan:
1) Hat keine Homologen mit einer geringeren Anzahl von Kohlenstoffatomen
2) ist flüssig
3) ist ein Gas bei Raumtemperatur
4) hat ein kleineres relatives Molekulargewicht als Luft
5) hat keine Isomere
6) löst sich in Wasser auf
4. Bei der Interaktion von 1 Mol Methan mit 3 Mol Chlor wird gebildet:
1) 1 Mol Trichlormethan
2) 1 Mol Trichlormethan und 3 Molchlorid
3) 1 Mol Trichlormethan und 2 Mol Chlorid
4) 3 Mol Trichlormethan und 3 Molchlorid
5. Die Ethan-Dehydrierung betrifft Reaktionen:
1) endothermisch.
2) Zersetzung.
3) Beitritt.
4) katalytisch
5) exotherme.
6) nicht katalitant
6. Bestimmen der molekularen Formel des Begrenzungskohlenwasserstoffs, wobei die Wechselwirkung von 1,74 g mit 4,11 g des Monobromderivats mit Brom gebildet ist.
3 Option
1. Strukturelle Formel von Alkan:

2. Homologen sind Substanzen, deren Namen sind:
1) 2-Methylpenan und 2-methylbutan
2) 2-Methylpropan und Butan
3) 2,2-Dimethylbutan und 2-methylpenan
4) Bhutan und Cyclobutan
3. Verny Lüge folgende Urteile Auf den physikalischen Eigenschaften von Alkanen?
A. alle Alkanen -Gaso-förmigen oder flüssigen Substanzen.
B. Alkane sind in Wasser gut löslich.
1) ist nur wahr
2) True nur b
3) Beide Urteile sind wahr
4) Beide Urteile sind falsch
4. Mit der Zersetzung von Methan nicht Gebildet:
1) Wasserstoff
2) Ethylen.
3) Acetylen.
4) Verkauf.
5. Für Ethan charakteristisch für die Reaktion:
1) mit Wasserstoff
2) mit Sauerstoff
3) mit Natriumhydroxidlösung
5) Mit Brom
6) mit konzentrierter Schwefelsäure
6. Bei der Werden einer molekularen Formel eines Dibromolomans mit 85,11% Brom.
Antworten auf prüfung in der Chemiealkana.
1 Option
1. 4
2. 2
3. 1
4. 4
5. 3
6. 299,52
Option 2
1. 1
2. 3
3. 35
4. 2
5. 124
6. C 4 H 10
3 Option
1. 1
2. 1
3. 4
4. 2
5. 25
6. C 2 H 4 BR 2
Testen am Thema "Alkaans" Option 1.
Teil A.
A 1. Allgemeine Formel Homologische Serie von Alkanov:
A 2. Die Anzahl der Elemente in Substanz Bhutan ist:
1. 1 2. 2 3. 3 4. 4
Und 3. Homologen sind:
1. Hexan und Hexanal. 2. Hexan und Hexen. 3. Bhutan und Pentan. 4.Butan und Pentyl.
1. Ethan. 2. Propen 3. Butadien. 4. Pentina.
1. Hexan und Bhutan. 2. Cyclobutan und Cyclopropan. 3. Butan und 2-Methylbutan. 4. Butan und 2-Methylpropan.
1. Ethin 2. Isobutan. 3. Ethen. 4. Cyclopenten.
A 7. Die Anzahl der Kohlenstoffatome von 5,6 l (n. Y.) propan ist:
1. 5 . 1022 2. 1,5 . 1023 3. 0,1 . 1023 4. 4,5 . 1023
1. Isobutan 2. Butadien -1.3. 3. Propin. 4. Benzol.
1. 1 2. 2,3 3. 3 4. 4,6
Und 15. Allgemeine Formel der homologen Serie von Cycloalkanen:
1. Brometan. 2. Propanol. 3. 1.2 - DIBEROMETHAN. 4. 2,2,3,3 - Tetramethythan.
1. Propan 2. Bhutan 3. Ethan. 4. Ethylen.
Und 18. Die Masse (kg) von Tetrachlormethan, das von 64 kg Methan mit einer praktischen Ausbeute von 97,4% erhalten wird, ist:
1. 600 2. 300 3. 900 4. 1500
CH3 - CH - CH2 - CH3
1. 2 - Ethylpropan. 2. 3 - Ethylpropan. 3. 3 - Methylpenan. 4. 3 - Methylbutan.
Eine 20. Masse des Kohlenwasserstoffs (in Gramm), das durch Erhitzen von 48 g 2 - Bromobutan mit 7,67 g Natrium erhalten wird, ist:
1. 10 2. 19 3. 38 4.76
Teil
1. Hydrierungsreaktionen.
6. Brennen in der Luft.
1. NSLO4 2. HNO2 3. C3H8 4. HBRO3 5. BCl3
In der 4. Hydrolyse von Aluminiumcarbid (AL4C3), das Methan mit einem Volumen von 67,2 Litern (n.) Erhalten wurde. Die Masse des gebildeten Aluminiumhydroxids ist (in Gramm) ......
Name Allgemeine Formel
1. Pentan a cnh2n + 1
2. Butin B CNH2N + 2
3. Cyclopropan in CNH2N
4. Ethyl g cnh2n-2
Testen am Thema "Alkana" Option 2.
Teil A.
Zu jeder Aufgabe von Teil A werden mehrere Antworten gegeben, von denen nur einer wahr ist. Wählen Sie den sicheren, Ihrer Meinung nach die Antwort. Setzen Sie das Kreuz in dem Antwortformular an der Jobnummer in die Zelle, deren Anzahl der Anzahl der gewählten Antwort entspricht.
A 1. Allgemeine Formel der homologen Serie von Cycloalkanen:
1. CNH2N 2. CNH2N + 2 3. CNH2N-2 4. CNH2N-6
A 2. Die Anzahl der Elemente in der Substanzpentan ist:
1. 1 2. 2 3. 3 4. 4
Und 3. Homologen sind:
1. Hexan und Hexanal. 2. Propan und Bhutan. 3. Butan und Buten. 4.Butan und Pentyl.
A 4. Substitutionsreaktionen sind charakteristisch für:
1. Ethen. 2. Propin. 3. Butadien. 4. Pentan.
Und 5. Strukturalisomere sind:
1. Hexan und Bhutan. 2. Cyclobutan und Cyclopentan. 3. Butan und 2-Methylbutan. 4. Pentan und 2 - Methylbutan.
Und 6. In dem Molekül davon gibt es keine π-Kommunikation:
1. Ethin 2. Butadien. 3. Ethan. 4. Cyclopenten.
A 7. Die Anzahl der Kohlenstoffatome bei 11,2 Litern (n.) Propan ist:
1. 15 . 1022 2. 9 . 1023 3. 0,3 . 1023 4. 4,5 . 1023
Und 8. der Kohlenwasserstoff, in dem die Orbitalkohlenstoffatome SP3-Hybridisierung aufweisen - ist
1. Potin 2. Butadien -1.3. 3. Propan. 4. Benzol.
A 9. Die Massenfraktion von Wasserstoff ist der größte in Verbindung:
1. C4N8 2. C4N10 3. C6H6 4. C5H12
Und 10. 2 -Hlorin - 2 - Methylbutan interagiert mit
1. Chlorid. 2. konzentrierte Schwefelsäure. 3. Stickstoff. 4. Natriumhydroxid in Alkoholösung.
Ein 11. Volumen (in Liter, n. Y.) angetriebener Propan mit 3.6. 1023 Wasserstoffatome gleich:
1. 1,68 2. 13,44 3. 34,48 4. 53,25
Ein 12. am nächsten chemische Eigenschaften Sie haben beide Substanzen eingestellt:
1. Calcium- und Eisensulfate (II). 2. Propan und Bhutan. 3. Silizium- und Schwefeldioxide.
4. Ethylen und Acetylen.
Und 13. Im Schema der Transformationen ethanol → x → Bhutan-Substanz X ist:
1. Butanol - 1. 2. Ethen. 3. Chlorethan. 4. Ethan.
Eine 14. Masse (in Gramm) einer Mischung aus einem Gemisch, bestehend aus 1,12 Litern (n. Y. y.) methan und 2,24 l (n. Y. y. y. y.) ist gleich:
1. 1,8 2. 2,3 3. 3,6 4. 4,6
A 15. Allgemeine Formel der homologen Serie von Alkanans:
1. CNH2N + 2 2. CNH2N 3. CNH2N-2 4. CNH2N-6
Und 16. Die Reaktion der Spaltung (Eliminierung) ist nicht charakteristisch für:
1. Chlorhetan. 2. 1.2 - Dichlorethan. 3. 2,2,3,3 - Tetramethythan. 4. Propanel
A 17. Als Ergebnis der folgenden Transformationen
C + H2 → X1 → X2 → X3 → X4 → X5 Das Endprodukt wird gebildet (X5):
1. 1 - Bromutin. 2. Bhutan 3. 2-BROMBUTAN. 4. 2 - Brom-2 - Methylpropan.
Und 18. Die Masse (kg) von Tetrachlormethan, das aus 32 kg Methan mit einer praktischen Ausbeute von 94,2% ergab, ist:
1. 600 2. 290 3. 400 4. 150
A 19. Nennen Sie den Stoff auf der internationalen Nomenklatur des Juden:
CH2 - CH - CH2 - CH3
1. 1.2 - Dimethylbutan. 2. 3.4 - Diethylbutan. 3. 3 - Methylpenan.
4. 3 - Methylbutan.
Eine 20. Masse des Kohlenwasserstoffs (in Gramm), das beim Erhitzen von 129 g Chlorhetan mit 52 g Natrium erhitzt wird, ist:
1. 105 2. 58 3. 38 4.94
Teil
Die Antwort von Teil in möglicherweise kann eine ganze Zahl oder eine ganzzahlige Nummern sein, die in einer Reihe aufgenommen wurde, ohne Leerzeichen und Kommas sowie die Reihenfolge der Buchstaben. Die Fraktionen runden bis zu einer Ganzzahl auf, schreiben keine Einheiten.
In 1. Wählen Sie, ohne Leerzeichen und Kommas auszuwählen und aufzuschreiben, Merkmale für Methan:
1. Hydrierungsreaktionen.
2. Tetraedrale Molekülform.
3. Das Vorhandensein von π - Kommunikation im Molekül.
4. SP3 - Hybridisierung des Orbitalkohlenstoffatoms im Molekül.
5. Reaktionen mit Halogenwasserstoff.
6. Brennen in der Luft.
In 2. Platzieren Sie die Substanzen in der Reihenfolge der Erhöhung der Anzahl der Verbindungen im Molekül, schreibt die Zahlen ohne Räume und Kommas:
2. NSLO4 2. HNO2 3. C3H8 4. HBRO3 5. BCl3
In 3. Mit der Wechselwirkung von Ethan mit einem Volumen von 44,8 Liter (n.) Mit Salpetersäure wird Nitroetan mit einem Gewicht von 102 g und praktischer Leistung (in Prozent) erhalten ......
In der 4. Hydrolyse von Aluminiumcarbid (AL4C3), das Methan mit einem Volumen von 67,2 Litern (n.) Erhalten wurde. Die Masse des gebildeten Aluminiumhydroxids ist (in Gramm) ......
In 5. Installieren Sie die Korrespondenz zwischen den Säulen. Schalten Sie in strikter Übereinstimmung mit der Reihenfolge der ersten Spaltennummern die Buchstaben der ausgewählten Antworten aus der zweiten Spalte auf. Übertragen Sie die resultierende Reihenfolge von Buchstaben in das Antwortformular (ohne Zahlen, Kommas und Pass), beispielsweise ABBG.
Name Allgemeine Formel
1. Pentan a cnh2n + 1
2. Butin B CNH2N + 2
3. Cyclopropan in CNH2N
Testen am Thema "Alkana" variante 1.
Teil A.
A 1. Allgemeine Formel der homologen Serie von Alkanov:
A 2. Die Anzahl der Elemente in Substanz Bhutan ist:
1 2. 2 3. 3 4. 4
Und 3. Homologen sind:
Hexan und Hexanal. 2. Hexan und Hexen. 3. Bhutan und Pentan. 4.Butan und Pentyl.
Ethan. 2. Propen 3. Butadien. 4. Pentina.
1. Hexan und Bhutan. 2. Cyclobutan und Cyclopropan. 3. Butan und 2-Methylbutan. 4. Butan und 2-Methylpropan.
Ethina. 2. Isobutan. 3. Ethen. 4. Cyclopenten.
A 7. Die Anzahl der Kohlenstoffatome von 5,6 l (n. Y.) propan ist:
5 . 10 22 2. 1,5 . 10 23 3. 0,1 . 10 23 4. 4,5 . 10 23
Isobutan. 2. Butadien -1.3. 3. Propin. 4. Benzol.
C 3 H 8 2. C 4 H 10 3. C 6 H 6 4. C 5 H 12
Ein 10. 2 -brom-2 -methylbutan interagiert mit
1. konzentrierte Schwefelsäure. 2. Stickstoff. 3. Chlorid. 4. Kaliumhydroxid in Alkoholösung.
Ein 11. Volumen (in Liter, n. Y.) -Tabriken von Ethan enthaltend 7.224. 10 23 Wasserstoffatome sind:
26,88 2. 13,44 3. 4,48 4. 53,2
Kalzium- und Mangansulfate (II). 2. Ethan und Propan. 3. Silizium- und Schwefeldioxide.
4. Ethylen und Acetylen.
Butanol - 1. 2. BROMETAN. 3. Ethan. 4. Ethylen.
Eine 14. Masse (in Gramm) einer Mischung aus einem Gemisch, bestehend aus 2,24 Liter (n. Y. y.) methan und 1,12 l (n. Y. y. y. y.) ist gleich:
1 2. 2,3 3. 3 4. 4,6
Und 15. Allgemeine Formel der homologen Serie von Cycloalkanen:
Brometan. 2. Propanol. 3. 1.2 - DIBEROMETHAN. 4. 2,2,3,3 - Tetramethythan.
Propan. 2. Bhutan 3. Ethan. 4. Ethylen.
Und 18. Die Masse (kg) von Tetrachlormethan, das von 64 kg Methan mit einer praktischen Ausbeute von 97,4% erhalten wird, ist:
600 2. 300 3. 900 4. 1500
CH 3 - CH - CH 2 - CH 3
2 - Ethylpropan. 2. 3 - Ethylpropan. 3. 3 - Methylpenan. 4. 3 - Methylbutan.
Eine 20. Masse des Kohlenwasserstoffs (in Gramm), das durch Erhitzen von 48 g 2 - Bromobutan mit 7,67 g Natrium erhalten wird, ist:
10 2. 19 3. 38 4.76
Teil
Hydrierungsreaktionen.
Das Vorhandensein von π - Kommunikation im Molekül.
Reaktionen mit Halogenwasserstoff.
Brennen in der Luft.
Name Allgemeine Formel
Pentan a c n h 2n + 1
BATIN B C N H 2N + 2
Cyclopropan in c n h 2n
Ethyl g c n h 2n-2
Testen am Thema "Alkana" option 2.
Teil A.
Zu jeder Aufgabe von Teil A werden mehrere Antworten gegeben, von denen nur einer wahr ist. Wählen Sie den sicheren, Ihrer Meinung nach die Antwort. Setzen Sie das Kreuz in dem Antwortformular an der Jobnummer in die Zelle, deren Anzahl der Anzahl der gewählten Antwort entspricht.
A 1. Allgemeine Formel der homologen Serie von Cycloalkanen:
Mit n h 2n 2. c n h 2n + 2 3. c n h 2n-2 4. c n h 2n-6
A 2. Die Anzahl der Elemente in der Substanzpentan ist:
1 2. 2 3. 3 4. 4
Und 3. Homologen sind:
Hexan und Hexanal. 2. Propan und Bhutan. 3. Butan und Buten. 4.Butan und Pentyl.
A 4. Substitutionsreaktionen sind charakteristisch für:
Ethena. 2. Propin. 3. Butadien. 4. Pentan.
Und 5. Strukturalisomere sind:
1. Hexan und Bhutan. 2. Cyclobutan und Cyclopentan. 3. Butan und 2-Methylbutan. 4. Pentan und 2 - Methylbutan.
Und 6. In dem Molekül davon gibt es keine π-Kommunikation:
Ethina. 2. Butadien. 3. Ethan. 4. Cyclopenten.
A 7. Die Anzahl der Kohlenstoffatome bei 11,2 Litern (n.) Propan ist:
15 . 10 22 2. 9 . 10 23 3. 0,3 . 10 23 4. 4,5 . 10 23
Und 8. Kohlenwasserstoff, in dem die Orbitalkohlenstoffatome SP 3-Hybridisierung aufweisen - dies
Potno. 2. Butadien -1.3. 3. Propan. 4. Benzol.
A 9. Die Massenfraktion von Wasserstoff ist der größte in Verbindung:
C 4 H 8 2. C 4 H 10 3. C 6 H 6 4. C 5 H 12
A 10. 2 -Hlllor - 2 -Methylbutan interagiert mit
1. Chlorid. 2. konzentrierte Schwefelsäure. 3. Stickstoff. 4. Natriumhydroxid in Alkoholösung.
Ein 11. Volumen (in Liter, n. Y.) angetriebener Propan mit 3.6. 10 23 Wasserstoffatome sind:
1,68 2. 13,44 3. 34,48 4. 53,25
A 12. Die nächstgelegenen chemischen Eigenschaften haben beide Substanzen:
Calcium- und Eisen (ii) Sulfate. 2. Propan und Bhutan. 3. Silizium- und Schwefeldioxide.
4. Ethylen und Acetylen.
Und 13. Im Schema der Transformationen ethanol → x → Bhutan-Substanz X ist:
Butanol - 1. Ethten. 3. Chlorethan. 4. Ethan.
Eine 14. Masse (in Gramm) einer Mischung aus einem Gemisch, bestehend aus 1,12 Litern (n. Y. y.) methan und 2,24 l (n. Y. y. y. y.) ist gleich:
1,8 2. 2,3 3. 3,6 4. 4,6
A 15. Allgemeine Formel der homologen Serie von Alkanans:
Mit n h 2n + 2 2. c n h 2n 3. c n h 2n-2 4. c n h 2n-6
Und 16. Die Reaktion der Spaltung (Eliminierung) ist nicht charakteristisch für:
Chlorhetan. 2. 1.2 - Dichlorethan. 3. 2,2,3,3 - Tetramethythan. 4. Propanel
A 17. Als Ergebnis der folgenden Transformationen
C + h 2 → x 1 → x 2 → x 3 → x 4 → x 5 Das Endprodukt ist gebildet (x 5):
1 - Bromutan. 2. Bhutan 3. 2-BROMBUTAN. 4. 2 - Brom-2 - Methylpropan.
Und 18. Die Masse (kg) von Tetrachlormethan, das aus 32 kg Methan mit einer praktischen Ausbeute von 94,2% ergab, ist:
600 2. 290 3. 400 4. 150
A 19. Nennen Sie den Stoff auf der internationalen Nomenklatur des Juden:
CH 2 - CH - CH 2 - CH 3
1.2 - Dimethylbutan. 2. 3.4 - Diethylbutan. 3. 3 - Methylpenan.
3 - Methylbutan.
Eine 20. Masse des Kohlenwasserstoffs (in Gramm), das beim Erhitzen von 129 g Chlorhetan mit 52 g Natrium erhitzt wird, ist:
105 2. 58 3. 38 4.94
Teil
Die Antwort von Teil in möglicherweise kann eine ganze Zahl oder eine ganzzahlige Nummern sein, die in einer Reihe aufgenommen wurde, ohne Leerzeichen und Kommas sowie die Reihenfolge der Buchstaben. Die Fraktionen runden bis zu einer Ganzzahl auf, schreiben keine Einheiten.
In 1. Wählen Sie, ohne Leerzeichen und Kommas auszuwählen und aufzuschreiben, Merkmale für Methan:
Hydrierungsreaktionen.
Tetraedrale Molekülform.
Das Vorhandensein von π - Kommunikation im Molekül.
SP 3 - Hybridisierung des Kohlenstoffatoms Orbital im Molekül.
Reaktionen mit Halogenwasserstoff.
Brennen in der Luft.
In 2. Platzieren Sie die Substanzen in der Reihenfolge der Erhöhung der Anzahl der Verbindungen im Molekül, schreibt die Zahlen ohne Räume und Kommas:
NSLO 4 2. HNO 2 3. C 3 H 8 4. HBRO 3 5. BCl 3
In 3. Mit der Wechselwirkung von Ethan mit einem Volumen von 44,8 Liter (n.) Mit Salpetersäure wird Nitroetan mit einem Gewicht von 102 g und praktischer Leistung (in Prozent) erhalten ......
In der 4. Hydrolyse von Aluminiumcarbid (Al 4 C 3) wurde Methan mit einem Volumen von 67,2 Litern (n. Y.) erhalten. Die Masse des gebildeten Aluminiumhydroxids ist (in Gramm) ......
In 5. Installieren Sie die Korrespondenz zwischen den Säulen. Schalten Sie in strikter Übereinstimmung mit der Reihenfolge der ersten Spaltennummern die Buchstaben der ausgewählten Antworten aus der zweiten Spalte auf. Übertragen Sie die resultierende Reihenfolge von Buchstaben in das Antwortformular (ohne Zahlen, Kommas und Pass), beispielsweise ABBG.
Name Allgemeine Formel
Pentan a c n h 2n + 1
BATIN B C N H 2N + 2
Cyclopropan in c n h 2n
Staatliche budgetarische pädagogische Institution
Sekundäre schule № 336
Nevsky-Bezirk von St. Petersburg
Alkans, Cycloalkanes.
entwicklung von Testtests in der Chemie
für den Grad 10.
Entwickelt:
Samokhvalov Andrey Sergeevich. ,
Biologie- und Chemielehrer
Gbou Sosh №336 Nevsky Bezirk
St. Petersburg
2015 Jahr.
Testkontrolle auf den Themen: "Alkaans", "Cycloalkanes"
einer). Kommunikation im Alkanmolekül:
aber). doppelt; b). verdreifachen; im). Hälfte; d). Single?
2). Geben Sie die molekulare Formel von Ethan an:
aber). C 8 h 18; b). C 6 h 6; im). C 6 H 5 CH 3; d). C 2 h 6?
3). Geben Sie die Formel eines Stoffes an, der sich mit der Klasse "Alkana" bezieht:
aber). C 4 h 10; b). C 6 h 12; im). C 6 h 6; d). C 13 h 26?
vier). Allgemeine Formel der homologen Serie von Alkanes:
aber). C n h 2 n; b). C n h 2 n - 2; im). C n h 2 n - 6; d). C n h 2 n + 2?
fünf). Erdgas enthält hauptsächlich:
aber). Propan; b). Butan; im). Methan; d). Wasserstoff?
6). Welcher Kohlenwasserstoff ist ein Homolog von Bhutan:
aber). Ethylen; b). Benzol; im). Pentan; d). Isobutan?
7). Molekül-Methan-Form:
aber). Kegel; b). Kuba; im). Pyramiden; d). Tetraeder?
acht). Für Alkane ist Hybridisierung charakteristisch:
aber). SP 3; b). Sp; im). SP 2; d). SP 4?
neun). Der Winkel zwischen Kohlenstoffatomen in Alkanmolekülen ist:
aber). 120 °; b). 109 °; im). 90 °; d). 110 °?
10). Radikal ist:
aber). Gruppe von Atomen mit ungepflegten Elektronen;
b). Eine Gruppe von Atomen, die sich von Methan bis-ch 2 - unterscheiden;
im). Eine Gruppe von Atomen, die positiv aufgeladen sind;
d). Eine Gruppe von Atomen namens Functional?
elf). Formeln Nur Alkanov werden in Folge aufgezeichnet:
aber). C 3 H 6, C 2 H 4, C 6 H 14; b). C 4 H 10, C 2 H 6, C 3 H 8;
im). C 2 H 2, C 3 H 8, C 6 H 6; d). C 6 H 6, C 4 H 8, C 2 H 6?
12). Die Reaktion, die zur Dehnung der Kohlenstoffkette führt, ist:
aber). Nurez-Reaktion; b). Konovalov-Reaktion;
im). Die Reaktion der Isomerisierung von Alkanen; d). Hydrierungsreaktion von Alkenen?
13). Während der thermischen Zersetzung von Methan, wobei sie gleichzeitig auf 1500 ° C erhitzt und mit Wasser gekühlt werden, werden sie gebildet:
aber). C und h 2; b). C 2 h 2 und h 2; im). CO 2 und H 2; d). CO und H 2?
vierzehn). Für Alkane ist das Isomerismus charakteristisch: aber). die Positionen einer mehrfachen Kommunikation; b). Kohlenstoffskelett; im). geometrisch; d). Bestimmungen der Funktionsgruppe? fünfzehn). Für Alkanovnicht charakteristisch Reaktion: aber). Polymerisation; b). Isomerisierung; im). thermische Zersetzung; d). Auswechslung?
Sechszehn). Die Molmasse von Cycloalkan, die 6 Kohlenstoffatome in einem Molekül enthielt, ist gleich G / Mol:
ABER). 70; b). 48; im). 86; d). 84?
17). Für Cyclohexan ist die Reaktion nicht charakteristisch:
aber). Beitritt; b). Isomerisierung; im). Auswechslung; d). Verbrennung?
achtzehn). Was ist die Beziehung charakteristisch von Alkanans und Cycloalkans:
aber). ionisch; b). Kovalente nichtpolare; im). Wasserstoff; d). Kovalente Polar?
neunzehn). Die Summe aller Koeffizienten in der Cyclopropan-Verbrennungsreaktionsgleichung ist:
ABER). elf; b). fünfzehn; im). 23; d). 25?
zwanzig). Mit Wirkung mit einem Metallzink (beim Erhitzen) werden 1, 5-Dibrompenants erhalten:
aber). Cyclohexan; b). Pentan; im). Methylcyclopentan; d). Cyclopentan?
Antworten
Kriterien zur Schätzung der Teststeuerung
"5" - 17 - 19 Richtige Antworten;
"4" - 14 - 16 Richtige Antworten;
"3" - 9 - 13 Richtige Antworten;
"2" - 8 und weniger richtige Antworten.
LITERATURVERZEICHNIS
Anisimova K.a., Koltsova A.m. Chemie-Tests für 8 - 11 Klassen, Ivanovo: IPKPPK, 2013. - 268 p.
GARA N.N., ZUEVA M.V. Sammlung von Aufgaben zur Zwischenzertifizierung: 8 - 11 Klassen: ein Buch für einen Lehrer. - M.: Erleuchtung, 2013. - 368 s., Ill.
Surovtseva R.P., Gusey L.S., die verbleibenden N.I., Tatur A.O. Chemie-Tests für 10 - 11 Klassen: Lehranleitung. - M.: Tropfen, 2013. - 126 p, krank.
Chunikhinina L.l. 500 Chemie-Tests für 10 - 11 Klassen (für unabhängige Arbeit in der Schule und zu Hause). - M.: Pubds-Schule, 2012. - 86 p.
Test auf dem Thema: "Alkans"
2 Konten für 14 Fragen

1. Der erste Vertreter einer Reihe von Alkanans wird aufgerufen:
a) Bhutan; b) Propan; c) Octan; d) Methan.
2. Allgemeine Formel von Alkanov:
wie. n. H 2. n. ; b) S. n. H 2. n. +2; c) S. n. H 2. n. -2; d) S. n. H. n. .
3. Kohlenstoffatome in Alkanen sind in einem Zustand:
aber) sP. -Hybridisierung;
b) pr. -Hybridisierung;
im) sP. 3-Hybridisierung;
d) in einem nichtregistern Zustand.

4. Der Valenzwinkel in Alkanes ist:
a) 109 ° 28 "; b) 180 °; c) c) 90 °; g) 270 °.
5. Molekül von Methan hat eine Struktur:
a) Oktaedral; b) Ebene;
c) tetraedral; d) hexagonal.
6. Kommunikation im Alkanmolekül:
aber). doppelt; b). verdreifachen;
im). Hälfte; d). Single.

7. Jeder nachfolgende Vertreter der homologen Reihe organischer Verbindungen unterscheidet sich von der vorherigen homologen Differenz gleich:
a) Sn; b) CH 3; c) CH 4; d) CH 2.
8. Erdgas enthält hauptsächlich:
aber). Propan; b). Butan; im). Methan; d). Wasserstoff.
9 . Radikal ist:
aber). Gruppe von Atomen mit ungepflegten Elektronen;
b). Eine Gruppe von Atomen, die sich von Methan bis-CH 2 unterscheiden;
im). Eine Gruppe von Atomen, die positiv aufgeladen sind;
d). Eine Gruppe von Atomen namens Functional.

10. Um einem Radikal einen Namen zu geben, müssen Sie im Namen von Alkan auf:
a) -in; b) -il; c) -n; d) -dien.
11. Welche der obigen Substanzen sind Isomere?
1) CH 3 - (CH 2) 5 -CH 3; 2) CH 3 -CH (CH 3) - C (CH 3) 2 -CH 3;
3) CH 3 -C (CH 3) 2 -CH 3; 4) CH 3 -CH (CH 3) - SH (CH 3) -CH 3.
a) 1 und 2; b) 1 und 4; c) 2 und 4; d) 3 und 4.
12. Welcher Kohlenwasserstoff ist ein Homolog von Bhutan:
aber). Ethylen; b). Benzol; im). Pentan; d). Isobutan.

13. Substanz CH 3 -CH (CH 3) - SH (CH 3) -CH 3 heißt:
a) 2,3,4-Trimethylochan; b) n. -Hexan;
c) 2,3-Dimethylbutan; d) 3,4-Dimethylpenan.
14. Der siebte Vertreter einer Reihe von Alkanans heißt: a) Octan; b) Nonan;
c) Dekan; d) Heptan.
15 . Für Alkane ist das Isomerismus charakteristisch:
aber). die Positionen einer mehrfachen Kommunikation;
b). Kohlenstoffskelett;
im). geometrisch;
d). Positionen der funktionellen Gruppe

16. Um einen verzweigten Kohlenwasserstoff anzurufen, benötigen Sie zuerst:
a) Wählen Sie die längste Kette von Kohlenstoffatomen;
b) Geben Sie die Namen der Radikale an;
c) angeben, die zur Klasse der Substanzen gehören;
d) Geben Sie den Ort der Radikale an.
17. Substanzen CH 3 -CH 3 und CH 3 -CH 2 -CH 3 sind:
a) Isomere; b) Homologe;
c) allotrope Modifikationen;
d) Radikale.

18. Gasförmige Alkane sind:
a) CH 4, C 4 H 10 von 10 h 22;
b) C 3 H 8, C 2 H 6 mit 4 H 10;
c) von 6 h 14 mit 5 h 12 von 5 h 10;
d) C 7 H 16, C 6 H 14 von 10 h 22.
19. Reaktion
2sn 3 I + 2na \u003d 2nai + c 2 N. 6
tragen Sie einen Namen:
a) n.n.zinin; b) A.m. Butlerova;
c) sh.a. lyursa; d) d.i. inendeeva.

20. Pentan-Formel:
a) mit 4 h 10; b) von 5 h 10; c) mit 5 h 12; d) von 10 h 22.
21. Formel C 2 H 5 Übereinstimmungen:
a) radikale Ethyl; b) Dean;
c) Ethan; d) Bhutan.
22. Die Wechselwirkung von Methan mit Chlor ist die Reaktion:
a) Zersetzung; b) Verbindungen;
c) Austausch; d) Substitution.

23. Tetrachlormethan-Formel:
a) ccl 4; b) SNSL 3; c) CH 2 SL 2; d) CH 3 SL.
24. Aus der nachstehenden Reaktion wählen Sie die durch den freien Radikalmechanismus fließenden Reaktion aus:
a) CH 4 → C + 2n 2;
b) ab 2N 5 er + hbr → C 2 H 5 BR + H 2 O;
c) CH 4 + BR 2 → Mit H 3 BR + H BR;
d) Sn 4 + N 2 O → Co + 3h 2.
25. Methan-Monochlorinierungsprodukt:
a) CH 2 SL 2; b) SNSL 3; c) cl 4; d) CH 3 CL.

26. Während der thermischen Zersetzung von Methan, wobei sie gleichzeitig auf 1500 ° C erhitzt und mit Wasser gekühlt werden, werden sie gebildet:
aber). C und h 2; b). C 2 h 2 und h 2; im). CO 2 und H 2; d). CO und H 2
27. Für Alkanov nicht charakteristisch Reaktion :
aber). Polymerisation; b). Isomerisierung;
im). thermische Zersetzung; d). Auswechslung?
28. Die Summe aller Koeffizienten in der Methanbrennreaktionsgleichung ist:
aber). 2; b) .4; um 6; d). acht?

Kriterienwerte:
14 punkte "fünf"
11- 13 punkte "Vier"
7-10 punkte "3"