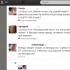
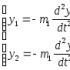«به دست آوردن، جمع آوری و شناخت گازها».
تحولات کار عملی برای کلاس 11 ارائه شده است
” کار عملی شماره 2 - پایه یازدهم ”
کار عملی شماره 2
شناسایی مواد معدنی
هدف کار : استفاده از واکنشهای مشخصه برای تشخیص پیشنهاد
مواد معدنی، ترکیب کیفی خاک را تعیین می کند.
تجهیزات :
معرف ها :
پیش رفتن :
جدولی برای ثبت اتمام کار به شکل زیر تهیه کنید:
| کاری که آنها انجام می دادند | مشاهدات | معادلات واکنش | |
2. انجام آزمایش
3. جدول را پر کنید.
4. یک نتیجه کلی بگیرید.
مقررات ایمنی
با اسیدها و قلیاها به دقت کار کنید. اسیدهای غلیظ را با احتیاط داخل یک لوله آزمایش روی سینی اضافه کنید. اگر اسید روی پوست یا لباس شما میرسد، سریعاً با آب فراوان بشویید.
طعم چیزی را نچشید.
بیش از 1 میلی لیتر از مواد را در لوله آزمایش بریزید.
مواد فرار را با دقت بو کنید و هوا را با دست از لوله آزمایش به سمت خود هدایت کنید.
هنگام تکان دادن مایع داخل لوله آزمایش با انگشت خود آن را نپوشانید. محتویات باید با نگه داشتن لوله آزمایش از بالا و تکان دادن کمی تکان داده شود.
روی لوله آزمایش خم نشوید زیرا ممکن است پاشش به چشم شما وارد شود.
لوله آزمایش را با مایع گرم شده و سوراخ آن را از خود و دوستانتان دور نگه دارید، زیرا گاهی اوقات ممکن است مایع از لوله آزمایش خارج شود.
هنگام گرم کردن لوله آزمایش، به فتیله لامپ الکل دست نزنید، زیرا فتیله سرد است و ممکن است لوله آزمایش پاره شود.
لامپ الکلی در حال سوختن را نمی توان از یک میز به میز دیگر منتقل کرد.
چراغ روح را فقط با کبریت روشن کنید.
لامپ الکلی را فقط با درپوش خاموش کنید.
بعد از کار، محل کار خود را مرتب کنید.
تجربه. واکنش های کیفی به مواد معدنی.
ورزش: در سه لوله آزمایش شماره گذاری شده (1، 2، 3) مواد زیر آورده شده است:
کلرید آمونیوم
اسید هیدروکلریک
سولفات سدیم
با استفاده از واکنش های مشخصه، تشخیص دهید که کدام لوله آزمایش حاوی این مواد است.
برای انجام این آزمایش، محتویات هر لوله آزمایش شماره گذاری شده را به سه نمونه تقسیم کنید.
1. برای تعیین کلرید آمونیوم، محلول هیدروکسید سدیم را به یک لوله آزمایش با کلرید آمونیوم اضافه کنید و آن را در شعله لامپ الکلی گرم کنید.
چه چیزی را مشاهده می کنید؟
2. برای تعیین اسید کلریدریک، محلول نیترات نقره را در لوله آزمایش با اسید کلریدریک بریزید.
چه چیزی را مشاهده می کنید؟
معادله واکنش را به صورت مولکولی، یونی کامل و یونی احیا شده بنویسید.
3. برای تعیین سولفات سدیم، محلول کلرید باریم را به یک لوله آزمایش با سولفات سدیم اضافه کنید.
چه چیزی را مشاهده می کنید؟
4. معادله واکنش را به صورت مولکولی، یونی کامل و یونی مختصر بنویسید.
مشاهده محتویات سند
"کار عملی شماره 1-1"
کار عملی شماره 1
هدف کار :
تجهیزات و معرف ها:دستگاه برای به دست آوردن گازها، لوله های آزمایش (2 عدد)، پایه برای لوله های آزمایش، کاردک، بشر، ترکش، کبریت، سنگ مرمر (CaCO 3)، آب آهک (Ca(OH) 2)، HCl (1:2).

ملاحضات امنیتی: 


پیش رفتن :
| اقدامات | مشاهدات | معادلات واکنش نتیجه گیری |
| تولید دی اکسید کربن  | CaCO 3 + HCl → |
|
|
انتهای لوله خروجی گاز را به یک لوله آزمایش حاوی 1 میلی لیتر آب آهک منتقل کرده و دی اکسید کربن را از آن عبور دهید. معادلات واکنش های مربوطه را بنویسید. | Ca(OH) 2 + CO 2 → |
نتیجه :
مشاهده محتویات سند
"کار عملی شماره 1-2"
کار عملی شماره 1
"به دست آوردن، جمع آوری و شناخت گازها"
هدف کار :
تجهیزات و معرف ها: لوله آزمایش (3 عدد)، چراغ الکلی، کبریت، سه پایه، لوله خروجی گاز، کلرید آمونیوم (کریستالی)، هیدروکسید کلسیم (بلور)، لیوان آب، کاغذ نشانگر، پشم پنبه.


ملاحضات امنیتی
: 




پیش رفتن :
| اقدامات | مشاهدات | معادلات واکنش نتیجه گیری |
|
| NH 4 Cl + Ca (OH) 2 → NH4OH↔ |
نتیجه :
مشاهده محتویات سند
"کار عملی شماره 1-3"
کار عملی شماره 1
"به دست آوردن، جمع آوری و شناخت گازها"
هدف کار :
تجهیزات و معرف ها:لوله های آزمایش (2 عدد)، قفسه لوله آزمایش، کاردک، اسپلینتر، کبریت، پرمنگنات پتاسیم (KMnO 4)، کاغذ نشانگر.





ملاحضات امنیتی: 
پیش رفتن :
| اقدامات | مشاهدات | معادلات واکنش نتیجه گیری |
| به دست آوردن اکسیژن به دست آوردن اکسیژن.  | KMnO4 → |
|
| جمع آوری و شناخت دی اکسید کربن لوله آزمایش را به مدت 1 دقیقه با گاز پر کنید. یک ترکش در حال سوختن را در یک لیوان قرار دهید. تغییرات را رعایت کنید. | CxHy+O 2 → |
نتیجه :
مشاهده محتویات سند
"کار عملی شماره 1"
کار عملی شماره 1.
«به دست آوردن، جمع آوری و شناخت گازها».
اهداف درس:صحت جذب دانش در مورد مواد گازی، روش های تولید و شناخت آنها را بررسی کنید. به توسعه مهارت های انجام آزمایش ها، مشاهده و نتیجه گیری از آنچه می بینند ادامه دهند.
تجهیزات:کامپیوتر، ارائه درس، لوله های آزمایش، لامپ الکل، کبریت، خرده ها، لوله های شیشه ای. محلول ها: اسید هیدروکلریک، اسید استیک، پراکسید هیدروژن، آب آهک؛ روی، سنگ مرمر،
در طول کلاس ها.
I. آمادگی برای درس(آمادگی گروه های دانش آموزان، تجهیزات، کلاس را برای درس بررسی کنید؛ دانش آموزان غایب را در گزارش علامت بزنید؛ موضوع و اهداف درس را گزارش کنید).
II. جلسه توجیهی ایمنی
1. اسیدها چه تأثیری بر پوست و بافت انسان دارند؟ (اگر با پوست یا پارچه انسان تماس پیدا کند، اسیدها آنها را از بین می برند).
2. قلیاها چه تأثیری بر پوست و پارچه انسان دارند؟ (در صورت تماس با پوست یا پارچه انسان، قلیاها آنها را از بین می برند).
3. بنابراین، چگونه باید اسیدها و قلیاها را اداره کرد؟ (اسیدها و قلیاها باید با لوله و فقط به مقدار لازم مصرف شوند).
4. چراغ روح خود را از چه کسی می توانید روشن کنید؟ (چراغ الکلی را نمی توان از چراغ الکلی دیگر روشن کرد. فقط با کبریت روشن می شود.)
به شما یادآوری میکنم که باید با ظروف شیشهای با دقت زیادی برخورد کنید تا له نشوند یا نشکنند. تراشه های ناشی از شکستن ظروف شیشه ای بسیار تیز هستند و می توانند بریدگی های بسیار عمیقی ایجاد کنند.
III. دستورالعمل کار.
طبق دستورالعمل کار عملی را انجام خواهید داد.
مطابق با گزینه خود، نام کار عملی را ذکر کنید، هدف را تنظیم کنید، تجهیزات و معرف ها را شناسایی کنید. هنگام اتمام کار، حتماً اعمال و مشاهدات خود را شرح دهید، معادلات واکنش های شیمیایی را یادداشت کنید، از تاسیسات تولید گازی که به شما نشان داده شده است، نقاشی بکشید و نتیجه گیری را روی کار یادداشت کنید.
پس از اتمام کار، محل کار را تمیز کنید.
IV. تکمیل کار.
"دریافت، جمع آوری و شناخت اکسیژن."
"تولید، جمع آوری و شناخت دی اکسید کربن".
"تولید آمونیاک"
قوانین کار ایمن با مواد قلیایی را مرور کنید. هنگام انجام آزمایش شیمیایی از این قوانین پیروی کنید.
تولید، جمع آوری و شناخت آمونیاک
1) دو قاشق از هر آمونیوم کلرید و هیدروکسید کلسیم را در هاون قرار دهید. مخلوط را با یک سمباده خرد کنید. چه احساسی دارید؟
2) دستگاه را برای به دست آوردن آمونیاک جمع کنید: یک لوله آزمایش خشک را با ارتفاع بیش از ¼ از مخلوط آماده شده پر کنید، لوله آزمایش را با یک درپوش با یک لوله خروجی گاز ببندید، لوله آزمایش را در پایه سه پایه محکم کنید. با کمی تمایل به سمت درپوش. یک لوله خشک جمع آوری آمونیاک را روی لوله خروجی گاز قرار دهید، به سمت بالا. 
3) لوله آزمایش را با مخلوط گرم کنید.
4) کاغذ نشانگر مرطوب را نزدیک دهانه لوله آزمایش آمونیاک قرار دهید. 
5) گرمایش را متوقف کنید. لوله آزمایش را با آمونیاک خارج کنید، بدون اینکه آن را برگردانید، آن را با سوراخ پایین در یک لیوان آب پایین بیاورید. انتهای لوله گاز را با یک سواب پنبه ای مرطوب بپوشانید.
مشاهده محتویات سند
” کار عملی تجهیزات و معرف درجه یازدهم ”
کار عملی پایه یازدهم
| عنوان شغلی | تجهیزات و معرف ها |
|
| به دست آوردن و شناخت گازها | تجهیزات:با لوله آزمایش، لامپ الکلی، کبریت، ترکش، لوله اگزوز شیشه ای، پشم پنبه، کاردک ایستاده. معرف ها:محلول ها: اسید هیدروکلریک، اسید استیک، پراکسید هیدروژن، آب آهک؛ روی، سنگ مرمر، کلرید آمونیوم، هیدروکسید کلسیم کریستالی، کاغذ شاخص، پرمنگنات پتاسیم. |
|
| شناسایی مواد معدنی | تجهیزات : پایه با لوله آزمایش، چراغ الکلی، کبریت، نگهدارنده لوله آزمایش. معرف ها : محلول ها: کلرید آمونیوم، سولفات سدیم، هیدروکسید سدیم، کلرید باریم، اسید هیدروکلریک. کاغذ تورنسل آبی، روی، نیترات نقره. |
” کار عملی درس شیمی آلی پایه یازدهم ”
کار عملی شماره 1
"تعیین ترکیب کیفی مواد آلی"
هدف کار : یاد بگیرید که حضور کربن و هیدروژن را در مواد آلی تعیین کنید.
تجهیزات و معرف ها : پایه آزمایشگاهی با پا، لوله آزمایش، درپوش با لوله خروجی گاز، لوله آزمایش اضافی، لوله شیشه ای، چراغ الکلی، کبریت، پارافین، اکسید مس (II)، سولفات مس بی آب (II)، هیدروکسید کلسیم (آب آهک).
پیش رفتن.
شرح تجربه
مشاهدات
نتیجه گیری و معادلات واکنش
آزمایش شماره 1 "اکسیداسیون پارافین"
0.5 گرم پارافین و 1 گرم اکسید مس (II) در یک لوله آزمایش خشک قرار داده شد. لوله آزمایش را در پایه سه پایه در حالت افقی محکم کردیم. کمی سولفات مس بی آب (II) را در نزدیکی دهانه لوله آزمایش با استفاده از یک لوله شیشه ای قرار دهید. لوله آزمایش با یک درپوش با یک لوله خروجی گاز بسته شد که انتهای آن در یک لوله آزمایش دیگر با 1.5 - 2 میلی لیتر آب آهک غوطه ور شد.
محتویات لوله آزمایش با مخلوط در شعله یک لامپ الکلی حرارت داده شد و قبلاً پارافین را ذوب کرده بود.
اکسید
فلز مس ( II)"
نتیجه:
C 18 H 38 + CuO →
آزمایش شماره 2 "تعیین کربن"
محصولات تجزیه گازی پارافین از محلول آب آهک عبور داده شد.
نتیجه:
CO 2 + Ca(OH) 2 →
آزمایش شماره 3 "تعیین هیدروژن"
محصولات تجزیه پارافین از طریق سولفات مس بی آب (II) عبور داده شد.
نتیجه:
H 2 O + CuSO 4 →
نتیجه گیری کلی:
کار عملی شماره 2
تهیه و بررسی خواص اتیلن
هدف کار : اتیلن را بدست آورید و خواص آن را مطالعه کنید، واکنش های کیفی را روی پیوند دوگانه انجام دهید.
تجهیزات و معرف ها : پایه آزمایشگاهی با پا، یک لوله آزمایش، یک درپوش با یک لوله خروجی گاز، دو لوله آزمایش اضافی، یک چراغ الکلی، کبریت، قطعات ظروف چینی، الکل اتیلیک C 2 H 5 OH، اسید سولفوریک H 2 SO 4،
آب برم Br2، محلول پرمنگنات پتاسیم KMnO4.
پیش رفتن
شرح تجربه
مشاهدات
نتیجه گیری و معادلات واکنش
آزمایش شماره 1 "تولید اتیلن"
1 میلی لیتر اتیل الکل در یک لوله آزمایش خشک ریخته شد و 3 میلی لیتر اسید سولفوریک غلیظ به آن اضافه شد. برای اطمینان از جوشیدن یکنواخت، چند تکه چینی شکسته را به مخلوط اضافه کنید. لوله آزمایش را با یک درپوش با لوله خروجی گاز بسته و لوله آزمایش را در پایه سه پایه به صورت افقی محکم کردیم.
محتویات لوله آزمایش به همراه مخلوط را با دقت در شعله یک لامپ الکلی حرارت دادند تا بجوشد.
کم آبی بدن
الکل اتیلیک"
نتیجه:
آزمایش شماره 2 «برهم کنش اتیلن
بدون توقف حرارت دادن مخلوط، انتهای لوله خروجی گاز را داخل لوله آزمایشی با آب برم پایین آوردیم و اتیلن را از آن عبور دادیم.
با برم
اب"
نتیجه:
آزمایش شماره 3 "برهم کنش اتیلن
بدون توقف حرارت دادن مخلوط، انتهای لوله خروجی گاز را با محلول اسیدی پرمنگنات پتاسیم سرمه ای داخل لوله آزمایشی پایین آوردند و اتیلن را از آن عبور دادند.
با محلول
پتاسیم پرمنگنات"
نتیجه:
آزمایش شماره 4 "احتراق اتیلن"
بدون توقف حرارت دادن مخلوط، لوله خروجی گاز را به سمت بالا چرخانده و اتیلن آزاد شده را با استفاده از کبریت مشتعل کردیم.
نتیجه:
نتیجه گیری کلی:
کار عملی شماره 3
"حل مسائل محاسباتی و کیفی با موضوع "روابط ژنتیکی بین هیدروکربن ها، الکل ها، آلدئیدها، اسیدهای کربوکسیلیک"
هدف کار : بر اساس دانش خواص شیمیایی هیدروکربن ها و مشتقات حاوی اکسیژن آنها، حل مسائل محاسباتی و کیفی مربوط به اجرای اتصال ژنتیکی مواد آلی را بیاموزید.
تجهیزات و معرف ها : قفسه لوله آزمایش، لوله آزمایش، ماشین لباسشویی، شیشه تخلیه، لامپ الکلی، کبریت، جای لوله آزمایش، CuSO 4، NaOH، سیم مسی، متانول، اتانول، فرمالدئید.
پیش رفتن:
شرح آزمایشات
مشاهدات
نتیجه گیری و معادلات واکنش
تجربه شماره 1"تهیه آلدئیدها از
الف) دیواره های یک لوله آزمایش خشک را با الکل اتیلیک مرطوب کنید. سیم مسی را در شعله گرم کنید تا یک پوشش سیاه ظاهر شود. سیم داغ داخل لوله آزمایش آماده شده پایین آمد. تکرار شد.
الکل ها"
نتیجه:
ب) دیواره های لوله آزمایش خشک را با متیل الکل مرطوب کنید. سیم مسی را در شعله گرم کنید تا یک پوشش سیاه ظاهر شود. سیم داغ داخل لوله آزمایش آماده شده پایین آمد. تکرار شد.
نتیجه:
آزمایش شماره 2 «به دست آوردن کربن
8 قطره فرمالین به لوله آزمایش، 8 قطره NaOH و در حین تکان دادن، قطره قطره CuSO 4 اضافه می شود تا رسوبی ناپدید نشده ظاهر شود. حرارت داده تا بجوشد.
اسیدها از
آلدئیدها"
نتیجه:
نتیجه گیری کلی:
کار عملی شماره 4
"واکنش های کیفی به مواد آلی حاوی اکسیژن"
هدف کار : بر اساس دانش واکنش های کیفی، حل مسائل تجربی در شناخت مواد آلی را بیاموزید.
تجهیزات و معرف ها : پایه لوله آزمایش، لوله های آزمایش، فلاسک با آب، شیشه تخلیه، لامپ الکلی، کبریت، جای لوله آزمایش، CuSO 4، NaOH، سیم مسی، متیل اورانژ، مواد آلی در لوله های آزمایش.
ورزش:محلولها در چهار لوله آزمایش شمارهدار داده شدند: اتانول، فرمالین، گلیسیرین و اسید استیک. هر یک از مواد داده شده را به صورت تجربی تعیین کنید.
پیش رفتن:
شرح تجربه
مشاهدات
نتیجه گیری و معادلات واکنش
تجربه شماره 1" اثر متقابل در چهار لوله آزمایش، هیدروکسید مس (II) با واکنش سولفات به دست آمد
فلز مس ( II) با هیدروکسید سدیم و مواد اضافه شده به آن شماره 1، 2، 3، 4 مخلوط.
هیدروکسید
فلز مس ( II)"
نتیجه:
تجربه شماره 2 «تعامل با
لوله آزمایش با مواد شماره؟ و نه.؟ و هیدروکسید مس (II) از آزمایش شماره 1 در نگهدارنده لوله آزمایش تقویت شده و در شعله یک لامپ الکلی حرارت داده شد.
هیدروکسید
فلز مس ( II) هنگام گرم شدن"
نتیجه:
آزمایش شماره 3 "تعریف"
1 میلی لیتر از محلول ماده شماره در لوله آزمایش ریخته شد. و 1 قطره متیل اورنج اضافه کرد.
سرکه
اسیدها"
نتیجه:
آزمایش شماره 4 «تعریف
1 میلی لیتر از محلول ماده شماره در لوله آزمایش ریخته شد. سیم مسی در شعله یک لامپ الکلی گرم شد تا زمانی که یک پوشش سیاه ظاهر شد و در ماده مورد مطالعه پایین آمد.
اتانول"
نتیجه:
کار عملی "شناخت مواد آلی".
هدف:تکرار واکنش های کیفی مشخصه مواد آلی، تثبیت مهارت های آزمایش شیمیایی.
معرف ها و تجهیزات:مواد آزمایش (گلیسیرین، نشاسته، اسید سیتریک، گلوکز)، آب، محلول آمونیاک اکسید نقره، سولفات مس، هیدروکسید سدیم، ید، لامپ الکل، کبریت، لوله آزمایش، نگهدارنده لوله آزمایش.
پیش رفتن
وظیفه شماره 1موادی که از طریق واکنش های کیفی به شما داده می شود را شناسایی کنید نتایج را رسمی کنید و نتیجه گیری را تدوین کنید.
| ماده ای که باید تعیین شود | نتایج واکنش کیفی |
|
| 1. گلیسیرین CH 2 -CH-CH 2 / / / اوه اوه اوه | Cu(OH)2 | محلول گلیسیرات مس آبی روشن |
| 2.نشاسته (C6H10O5)n | محلول ید | محلول آبی |
| 3. اسید سیتریک | الف) نشانگر جهانی. ب) فلز ب) Na 2CO 3 | الف) نشانگر جهانی قرمز می شود ب) گاز آزاد می شود ب) گاز آزاد می شود |
| 4. گلوکز C6H12O6 | Cu(OH)2 Ag2O | رسوب قرمز بازیابی نقره از اکسید |
وظیفه شماره 2.به سوالات ارائه شده پاسخ دهید.
1. چه موادی در نتیجه هیدرولیز نشاسته به وجود می آیند؟
2. چگونه می توانید به طور تجربی ثابت کنید که ماده ای که به شما داده شده استیک اسید است؟
3. چرا ساکارز واکنش آینه نقره ای نشان نمی دهد؟
نتیجه گیری:
"کار عملی شماره 2"
کار عملی
"واکنش های تبادل یونی. هیدرولیز نمکها
هدف کار:مهارت های ترکیب واکنش های تبادل یونی را تثبیت کنید، علائم وقوع واکنش های تبادل یونی را تا انتها تکرار کنید. مفهوم "هیدرولیز نمک ها" را تقویت کنید. PH محلول های نمک را به صورت تجربی مطالعه کنید. تقویت مهارت های آزمایش شیمیایی و بازنگری قوانین ایمنی.
پیش رفتن
وظیفه شماره 1.آزمایشی بین محلول های الکترولیت انجام دهید. به پدیده های مشاهده شده توجه کنید.
الف) Na 2 CO 3 و H 2 SO 4 (گاز)
ب) BaCl 2 و H 2SO 4 ( رسوب قبل از میلاد مسیح )
ب) NaOH و CuSO4 (رسوب GC)
د) NaOH و H 2SO 4 (آب)
معادلات را به صورت مولکولی و یونی بنویسید.
وظیفه شماره 2.هیدرولیز محلول های نمکی
محلول های نمک را با یک نشانگر جهانی آزمایش کنید PH محلول نمک و محیط را با تغییر رنگ نشانگر جهانی تعیین کنید.
هیدرولیز محلول های نمکی
الف) Na 2CO 3
ب) NH 4Cl
ب) FeCl 3
نتایج را در یک جدول ارائه دهید.
| Na 2 CO 3 | NH4Cl | FeCl3 |
|
| پایه | |||
| نشانگر جهانی |
معادلات واکنش های هیدرولیز را بنویسید و نتیجه را بنویسید.
فضای کاری خود را مرتب کنید.
نتیجه گیری:
مشاهده محتویات سند
"کار عملی شماره 3"
کار عملی "تحلیل کیفی ترکیبات آلی"
دستورالعمل استفاده
هدف کار:ایجاد مهارت در تعیین کیفی کربن، هیدروژن و کلر در ترکیبات آلی
تجهیزات، مواد:شمع پارافین، جای لوله آزمایش، لوله آزمایش، لیوان، مارپیچ مسی، لامپ الکلی، دی کلرو اتان.
وظیفه شماره 1 تعیین کیفی کربن در ترکیبات آلی.
یک شمع پارافین روشن کنید. یک لوله آزمایش تمیز را داخل شعله شمع قرار دهید. چه چیزی را مشاهده می کنید؟ نتایج آزمایش را توضیح دهید.
وظیفه شماره 2 تعیین کیفی هیدروژن در ترکیبات آلی.شمع در حال سوختن را با یک لیوان تمیز و خشک بپوشانید. چه چیزی را مشاهده می کنید؟ نتایج آزمایش را توضیح دهید.
وظیفه شماره 3 تعیین کیفی کلر در ترکیبات آلی.
مارپیچ مسی را در شعله یک لامپ الکلی گرم کنید و آن را به مشتق آلکان کلرید اضافه کنید.
سپس لامپ الکلی را دوباره داخل شعله قرار دهید. چه چیزی را مشاهده می کنید؟
نتایج آزمایش ها را در جدول بنویسید. نتیجه گیری خود را فرموله و بنویسید.
| آنها چه کار می کردند؟ | چه چیزی را مشاهده کردید؟ | ||
کار عملی در شیمی
کلاس هشتم
کار عملی شماره 1 "تکنیک های جابجایی تجهیزات آزمایشگاهی"
جلسه توجیهی ایمنی
تجهیزات آزمایشگاهی
1. طراحی و اصل عملکرد سه پایه آزمایشگاهی (یک سه پایه را بکشید، اجزای آن را برچسب بزنید)
2. طراحی و اصل عملکرد یک چراغ روح (یک چراغ روح را بکشید، اجزای آن را نشان دهید)
3. ظروف شیشه ای (کشیدن لوله های آزمایش، فلاسک ها، بشر)
4- فیلتراسیون:
1. کاغذ صافی تهیه کنید.
2. کاغذ صافی را مرطوب کنید.
3. در یک قیف قرار دهید.
4. مایع روی یک میله شیشه ای ریخته می شود و آن را به سمت دیواره قیف می گیرد.
5. فیلتر از دیواره لیوان به سمت پایین جریان مییابد و نه به مرکز، تا پاشیده نشود.
در متن تعاریف فیلتر، رسوب و فرآیند فیلتراسیون را بیابید.
کار عملی شماره 2"مشاهدات یک شمع در حال سوختن"
تجربه 1. پدیده های فیزیکی هنگام سوختن شمع
یه شمع روشن کن. خواهید دید که چگونه پارافین در نزدیکی فتیله شروع به ذوب شدن می کند و یک گودال گرد را تشکیل می دهد. چه فرآیندی (فیزیکی یا شیمیایی) در اینجا در حال انجام است؟
یک لوله شیشه ای را که با زاویه قائم با انبرهای بوته خم شده است بردارید، یک سر آن را در قسمت وسط شعله قرار دهید و سر دیگر را داخل لوله آزمایش قرار دهید. چه چیزی را مشاهده می کنید؟
1. پارافین ذوب می شود. این ذوب یک فرآیند فیزیکی است.
2. دیواره های لوله آزمایش مه می شود - این تراکم است - یک فرآیند فیزیکی.
تجربه 2. تشخیص محصولات احتراق در شعله
با استفاده از انبر بوته، یک تکه قلع (2x2 سانتی متر) را از یک قوطی حلبی یا یک لام شیشه ای بردارید، آن را در ناحیه مخروط تیره شمع در حال سوختن قرار دهید و 3-5 ثانیه نگه دارید. به سرعت قلع (شیشه) را بلند کنید و به صفحه زیرین نگاه کنید. آنچه در آنجا ظاهر شد را توضیح دهید.
لوله آزمایش خشک را در نگهدارنده محکم کنید، آن را وارونه کنید و روی شعله نگه دارید تا مه شود. پدیده مشاهده شده را توضیح دهید.
به سرعت 2-3 میلی لیتر آب آهک را در همان لوله آزمایش بریزید. چه چیزی را مشاهده می کنید؟ یه توضیح بدید
1. یک لکه تیره (سیاه) ظاهر شده است - این دوده (کربن) است که در هنگام سوزاندن پارافین ایجاد می شود.
2. رطوبت روی دیواره های لوله آزمایش متراکم می شود. این باعث تغلیظ آب، یکی از محصولات احتراق پارافین می شود.
3. وقتی آب آهک را به لوله آزمایش اضافه می کنید، کدر می شود:
این نشان می دهد که دومین محصول احتراق پارافین دی اکسید کربن است.
تجربه 3. تاثیر هوا بر احتراق شمع
یک لوله شیشه ای را با انتهای کشیده شده در یک حباب لاستیکی فرو کنید، با فشار دادن آن با دست، هوا را در شعله شمع فروزان باد کنید. روشنایی شعله چگونه تغییر کرد؟
دو شمع را با استفاده از پارافین ذوب شده به مقوا (پلای وود، تخته سخت) وصل کنید. آنها را روشن کنید و یکی را با یک شیشه نیم لیتری و دیگری را با یک شیشه دو لیتری بپوشانید (می توانید لیوان هایی با ظرفیت های مختلف بردارید). در چه مواردی شمع بیشتر می سوزد؟ چرا؟
اگر مواد تشکیل دهنده شمع دارای فرمول C هستند، معادلات واکنش های احتراق را بنویسید. 16 H 34 و C 17 H 36.
1. روشنایی شعله با افزایش جریان اکسیژن افزایش یافت.
2. یک شمع در یک شیشه بزرگتر می سوزد زیرا حاوی اکسیژن بیشتری است.
کار عملی شماره 3"تحلیل خاک و آب"
آزمایش 1. تجزیه و تحلیل مکانیکی خاک
خاک را در لوله آزمایش قرار دهید (ستون خاک باید 2-3 سانتی متر باشد). آب مقطر را اضافه کنید که حجم آن باید 3 برابر حجم خاک باشد.
لوله آزمایش را با درپوش بسته و به مدت 1-2 دقیقه کاملا تکان دهید سپس از ذره بین استفاده کنید و رسوب ذرات خاک و ساختار رسوبات را مشاهده کنید. مشاهدات خود را شرح دهید و توضیح دهید.
ابتدا ذرات بزرگتر و سنگین شن و خاک رس رسوب می کنند، سپس ذرات کوچکتر، اما محلول برای مدت طولانی کدر می ماند - کوچکترین ذرات معلق هستند.
آزمایش 2. به دست آوردن محلول خاک و آزمایش با آن
یک فیلتر کاغذی آماده کنید و آن را داخل قیف متصل به حلقه سه پایه قرار دهید. یک لوله آزمایش تمیز و خشک زیر قیف قرار دهید و مخلوط خاک و آب به دست آمده در آزمایش اول را فیلتر کنید. مخلوط را نباید قبل از فیلتر کردن تکان داد. خاک روی فیلتر باقی می ماند و فیلتر جمع آوری شده در لوله آزمایش عصاره خاک (محلول خاک) است.
چند قطره از این محلول را روی یک بشقاب شیشه ای بریزید و با موچین آن را روی مشعل نگه دارید تا آب تبخیر شود. چه چیزی را مشاهده می کنید؟ توضیح.
دو کاغذ تورنسل (قرمز و آبی) بردارید، محلول خاک را با یک میله شیشه ای روی آنها بمالید. بر اساس نتایج مشاهدات خود نتیجه بگیرید.
1. پس از تبخیر آب، یک پوشش سفید روی لیوان باقی می ماند؛ این مخلوطی از موادی است که در حین هم زدن در آب حل می شود.
2. کاغذ تورنسل جهانی اگر محلول خنثی باشد رنگ آن تغییر نمی کند، اگر اسیدی باشد قرمز و اگر قلیایی باشد آبی می شود.
آزمایش 3. تعیین شفافیت آب
برای آزمایش به یک استوانه شیشه ای ته صاف شفاف با قطر 2-2.5 سانتی متر و ارتفاع 30-35 سانتی متر نیاز دارید.می توانید از استوانه اندازه گیری 250 میلی لیتری بدون پایه پلاستیکی استفاده کنید.
توصیه می شود ابتدا آزمایش را با آب مقطر و سپس با آب حوض انجام دهید و نتایج را با هم مقایسه کنید. سیلندر را روی متن چاپ شده قرار دهید و در آب مورد آزمایش بریزید و مطمئن شوید که متن از طریق آب قابل خواندن است. توجه داشته باشید که در چه ارتفاعی فونت را نمی بینید. ارتفاع ستون های آب را با خط کش اندازه گیری کنید. نتیجه گیری کن.
ارتفاع اندازه گیری شده سطح دید نامیده می شود.
اگر سطح دید کم باشد، مخزن به شدت آلوده است.
آزمایش 4. تعیین شدت بوی آب
فلاسک مخروطی را پر کنید 2
/
3
حجم آب مورد آزمایش را با درپوش (ترجیحاً شیشه) محکم ببندید و به شدت تکان دهید. سپس فلاسک را باز کنید و به خصوصیات و شدت بو توجه کنید. با استفاده از جدول 8، شدت بوی آب را در نقاط ارزیابی کنید.
از جدول شماره 8 (صفحه 183) استفاده کنید.
کار عملی شماره 4"علائم واکنش های شیمیایی"
آزمایش 1. کلسینه کردن سیم مسی و برهمکنش اکسید مس (II) با اسید سولفوریک
لامپ الکل را روشن کنید. سیم مسی را با انبر بوته بردارید و داخل شعله قرار دهید. بعد از مدتی سیم را از روی شعله بردارید و رسوبات سیاه رنگی که روی آن ایجاد شده است را روی یک کاغذ تمیز کنید. آزمایش را چندین بار تکرار کنید. رسوب سیاه به دست آمده را در لوله آزمایش قرار داده و محلول اسید سولفوریک را داخل آن بریزید. مخلوط را گرم کنید. چه چیزی را مشاهده می کنید؟
آیا با گرم شدن مس ماده جدیدی تشکیل شد؟ معادله یک واکنش شیمیایی را بنویسید و نوع آن را بر اساس تعداد و ترکیب مواد اولیه و محصولات واکنش تعیین کنید. چه علائمی از یک واکنش شیمیایی مشاهده کردید؟ آیا با واکنش اکسید مس (II) با اسید سولفوریک، ماده جدیدی تشکیل شد؟ نوع واکنش را بر اساس تعداد و ترکیب مواد اولیه و محصولات واکنش تعیین کنید و معادله آن را بنویسید.
1. هنگامی که سیم مسی گرم می شود، مس اکسید می شود و اکسید مس سیاه (II) تشکیل می شود. این یک واکنش ترکیبی است.
2. اکسید مس (II) حاصل در اسید سولفوریک حل می شود، محلول آبی می شود و سولفات مس (II) تشکیل می شود:
این یک واکنش مبادله ای است.
آزمایش 2. برهمکنش سنگ مرمر با اسید
1-2 قطعه سنگ مرمر را در یک لیوان کوچک قرار دهید. مقداری اسید کلریدریک داخل لیوان بریزید تا روی قطعات را بپوشاند. یک ترکش را روشن کنید و داخل لیوان بیاورید.
آیا هنگام واکنش سنگ مرمر با اسید، مواد جدیدی تشکیل می شود؟ چه علائمی از واکنش های شیمیایی مشاهده کردید؟ معادله واکنش شیمیایی را بنویسید و نوع آن را بر اساس تعداد و ترکیب مواد اولیه و محصولات واکنش نشان دهید.
1. سنگ مرمر حل شده در اسید کلریدریک، یک واکنش شیمیایی رخ داد:
آزمایش 3. برهمکنش کلرید آهن (III) با تیوسیانات پتاسیم
2 میلی لیتر از محلول کلرید آهن (III) را در یک لوله آزمایش بریزید، و سپس چند قطره محلول تیوسیانات پتاسیم KSCN - نمک اسید HSCN، با یک باقیمانده اسید SCN.-
.
چه علائمی با این واکنش همراه است؟ معادله و نوع واکنش آن را بر اساس تعداد و ترکیب مواد اولیه و محصولات واکنش بنویسید.
محلول قرمز روشن شد و تیوسیانات آهن (III) تشکیل شد.این یک واکنش مبادله ای است.
آزمایش 4. برهمکنش کربنات سدیم با کلرید کلسیم
2 میلی لیتر محلول کربنات سدیم را در یک لوله آزمایش بریزید. سپس چند قطره محلول کلرید کلسیم اضافه کنید. چه چیزی را مشاهده می کنید؟ معادله واکنش شیمیایی را بنویسید و نوع آن را بر اساس تعداد و ترکیب مواد اولیه و محصولات واکنش نشان دهید.
یک رسوب کریستالی سفید از سولفات باریم مشاهده می شود. این یک واکنش مبادله ای است.
کار عملی شماره 5تهیه محلول شکر و تعیین کسر جرمی آن در محلول
برای اندازه گیری 50 میلی لیتر آب مقطر از استوانه ای استفاده کنید و آن را در یک فلاسک مخروطی 100 میلی لیتری بریزید.
یک قاشق چای خوری شکر گرانول (یا دو عدد) را در مقیاس آزمایشگاهی وزن کنید، سپس آن را در یک فلاسک حاوی آب قرار دهید و با میله شیشه ای هم بزنید تا کاملا حل شود.
حال به قسمت محاسبات بروید. ابتدا کسر جرمی شکر موجود در محلول را محاسبه کنید. شما داده های لازم را دارید: جرم شکر، حجم آب، چگالی آب برابر با 1 گرم در میلی لیتر است.
کلاس نهم
کار عملی شماره 1"انجام زنجیره ای از دگرگونی های شیمیایی"
واکنشهایی را انجام دهید که در آن تبدیلهای شیمیایی پیشنهاد شده در زیر انجام میشوند (طبق گزینهها).
معادلات واکنش های مربوطه را بنویسید. واکنش های تبادل یونی را نیز به صورت یونی بنویسید.
انتخاب 1.
بیایید تبدیل های زیر را انجام دهیم:
گزینه 2.
گزینه 3.
گزینه 3.
کار عملی شماره 2"تهیه و خواص ترکیبات فلزی"
تمرین 1
در ریاضیات یک قانون وجود دارد - "اگر مکان عبارات تغییر کند مجموع تغییر نمی کند." آیا این در مورد شیمی صادق است؟ این را با آزمایش زیر بررسی کنید.
هیدروکسید آلومینیوم را با واکنش تبادلی آماده کنید و ماهیت آمفوتری آن را ثابت کنید. برای این کار می توانید از واکنشی استفاده کنید که معادله آن است
این واکنش را در دو نوع، با استفاده از حجم یکسانی از مواد اولیه در هر نوع انجام دهید: ابتدا محلولی از یک معرف دیگر را به صورت قطرهای به محلول یکی از مواد اولیه (معرف) اضافه کنید، سپس ترتیب وارد کردن معرفها را به آن تغییر دهید. واکنش. مشاهده کنید که در چه صورت رسوب تشکیل می شود و در چه صورت تشکیل نمی شود.
نتایج را توضیح دهید و معادلات واکنش های انجام شده به صورت مولکولی و یونی را یادداشت کنید.
وظیفه 2
برای تایید ترکیب کیفی کلرید کلسیم واکنش ها را انجام دهید. معادلات واکنش را به صورت مولکولی و یونی بنویسید.
وظیفه 3
تغییرات را طبق طرح زیر انجام دهید 1
:
1
برای انجام تبدیل دوم، از آب کلر استفاده کنید.
معادلات واکنش های مربوطه را بنویسید و آنها را از نقطه نظر اکسیداسیون- احیا در نظر بگیرید. انجام واکنش های کیفی برای تایید وجود محصولات واکنش. معادلات واکنش را به صورت مولکولی و یونی بنویسید.
وظیفه 4
سولفات آهن (II) را حداقل از سه راه بدست آورید. معادلات واکنش های تبادل یونی را به شکل های یونی و مولکولی بنویسید و واکنش های جانشینی را از نقطه نظر اکسیداسیون- احیا در نظر بگیرید.
وظیفه 5
برای تایید ترکیب کیفی سولفات آهن (II) واکنش ها را انجام دهید. معادلات واکنش های مربوطه را به صورت مولکولی و یونی بنویسید.
کار عملی شماره 3"مشکلات تجربی در شناخت و به دست آوردن مواد"
سه لوله آزمایشی که به شما داده شده است (گزینه های 1، 2 یا 3) حاوی مواد جامد و سه لوله دیگر (گزینه 4) حاوی محلول هایی از مواد هستند.
به طور آزمایشی تعیین کنید که کدام لوله آزمایش حاوی هر یک از موادی است که به شما داده شده است. معادلات واکنش های مربوطه را به صورت مولکولی و یونی بنویسید.
پس از این قسمت از کار، یک یا دو کار آزمایشی را از لیست زیر (طبق دستور معلم) تکمیل کنید.
انتخاب 1
الف) هیدروکسید سدیم؛
ب) کربنات پتاسیم؛
ج) کلرید باریم.
گزینه 2
الف) کربنات کلسیم؛
ب) سولفات سدیم؛
ج) کلرید پتاسیم.
گزینه 3
الف) نیترات باریم؛
ب) سولفات سدیم؛
ج) کربنات کلسیم.
گزینه 4
الف) کلرید سدیم؛
ب) کلرید آلومینیوم؛
ج) کلرید آهن (III).
وظیفه 1. به طور تجربی ثابت کنید که سولفات آهن، نمونه ای از آن به شما داده شد، حاوی ترکیبی از سولفات آهن (III) است. معادلات واکنش های مربوطه را به صورت مولکولی و یونی بنویسید.
وظیفه 2. اکسید آهن (III) را با شروع از کلرید آهن (III) بدست آورید. معادلات واکنش های مربوطه و معادله واکنش شامل الکترولیت و به شکل یونی را بنویسید.
وظیفه 3. محلولی از آلومینات سدیم را با شروع از کلرید آلومینیوم تهیه کنید. معادلات واکنش های انجام شده به صورت مولکولی و یونی را بنویسید.
وظیفه 4. سولفات آهن (II) را از آهن شروع کنید. معادلات واکنش های انجام شده را بنویسید و فرآیندهای ردوکس را تجزیه و تحلیل کنید.
کار عملی شماره 4کارهای آزمایشی با موضوع "زیرگروه اکسیژن"
وظیفه 1.برای تایید ترکیب کیفی اسید سولفوریک واکنش ها را انجام دهید. معادلات واکنش را بنویسید.
وظیفه 2. 1-2 گرانول روی را در یک لوله آزمایش قرار دهید و حدود 1 میلی لیتر اسید سولفوریک رقیق را داخل آن بریزید. چه چیزی را مشاهده می کنید؟ معادله واکنش را بنویسید و فرآیندهای ردوکس را در نظر بگیرید.
وظیفه 3. محلول سولفید سدیم را در دو لوله آزمایش بریزید. در یکی از آنها آب کلر و در دیگری آب برم بریزید. چه چیزی را مشاهده می کنید؟ مشاهدات خود را توضیح دهید معادلات واکنش های مربوطه را به صورت مولکولی و یونی بنویسید.
کلر و آب برم مواد اکسید کننده هستند، بنابراین در هر دو لوله آزمایش، سولفید به گوگرد اکسید می شود. محلول ها تغییر رنگ می دهند.
وظیفه 4. به شما سه لوله آزمایش با محلول داده شده است. تعیین کنید که کدام یک حاوی اسید هیدروکلریک، اسید سولفوریک و هیدروکسید سدیم است. معادلات واکنش های مربوطه را به صورت مولکولی و یونی بنویسید.
وظیفه 5. تعیین کنید که آیا نمک سفره حاوی سولفات است یا خیر. معادلات واکنش را به صورت مولکولی و یونی بنویسید.
وظیفه 6. با استفاده از واکنش های مشخصه، تعیین کنید که نمکی که به شما داده می شود سولفات، یدید یا کلرید است. معادلات واکنش های مربوطه را به صورت مولکولی و یونی بنویسید.
وظیفه 7. با شروع از اکسید مس (II) محلولی از سولفات مس (II) بدست آورید و سولفات مس کریستالی را از آن جدا کنید. معادلات واکنش های مربوطه را به صورت مولکولی و یونی بنویسید.
وظیفه 8. به شما سه لوله آزمایش با محلول های سولفات سدیم، سولفیت و سولفید سدیم داده شده است. تنها با استفاده از یک معرف، تعیین کنید که کدام لوله آزمایش حاوی هر ماده است. معادلات واکنش های مربوطه را به صورت مولکولی و یونی بنویسید.
کار عملی شماره 5کارهای آزمایشی با موضوع "زیرگروه های نیتروژن و کربن"
وظیفه 1.واکنش هایی را انجام دهید که می توان از آنها برای اثبات اینکه ماده ای که در ظروف در بسته به شما داده شده است استفاده کنید:
الف) کلرید آمونیوم؛
ب) کربنات سدیم؛
ج) نیترات آمونیوم؛
د) آمونیاک؛
ه) کربنات کلسیم؛
ه) سیلیکات سدیم.
وظیفه 2. به طور تجربی ثابت کنید که سولفات آمونیوم و نیترات آمونیوم را نمی توان قبل از اعمال این کودها در خاک با آهک مخلوط کرد و دلیل آن را توضیح دهید. معادلات واکنش را بنویسید.
وظیفه 3. به طور تجربی ثابت کنید که:
الف) کلرید آمونیوم حاوی یون NH است 4 + و Cl - ;
ب) سولفات آمونیوم حاوی یون NH است 4 + و SO 4 2- .
معادلات واکنش های انجام شده به صورت مولکولی و یونی را بنویسید.
وظیفه 4. آمونیاک را از نمک های زیر بدست آورید:
الف) کلرید آمونیوم؛
ب) سولفات آمونیوم؛
ج) نیترات آمونیوم.
معادلات واکنش های انجام شده به صورت مولکولی و یونی را بنویسید.
وظیفه 5. واکنش هایی را که با معادلات یونی خلاصه شده بیان می شوند، کار کنید.معادلات واکنش های انجام شده به صورت مولکولی و یونی را بنویسید.
وظیفه 6. در چهار لوله آزمایش به شما مواد کریستالی داده می شود: سولفات سدیم، کلرید روی، کربنات پتاسیم، سیلیکات سدیم. مشخص کنید که در هر لوله آزمایش چه ماده ای وجود دارد. معادلات واکنش را به صورت مولکولی و یونی بنویسید.
کار عملی شماره 6
انتخاب 1.
آزمایش 1. به دست آوردن، جمع آوری و شناخت هیدروژن
دستگاه را برای به دست آوردن گازها جمع آوری کنید و آن را از نظر نشتی بررسی کنید. 1-2 گرانول روی را در یک لوله آزمایش قرار داده و 1-2 میلی لیتر اسید کلریدریک داخل آن بریزید. لوله آزمایش را با یک درپوش با یک لوله خروجی گاز ببندید (شکل 43 را ببینید) و یک لوله آزمایش دیگر را روی نوک لوله قرار دهید. کمی صبر کنید تا لوله آزمایش با گاز آزاد شده پر شود.
لوله آزمایش را با هیدروژن بردارید و بدون معکوس کردن، آن را به لامپ الکل در حال سوختن بیاورید. اگر هیدروژن با یک انفجار کسل کننده منفجر شود، تمیز است، و اگر با صدای "پارس" منفجر شود، به این معنی است که هیدروژن با هوا ("گاز انفجاری") مخلوط شده است.
سوالات و وظایف
1. وقتی روی با اسید هیدروکلریک واکنش می دهد چه اتفاقی می افتد؟ معادله ای برای واکنش ایجاد کنید و آن را با استفاده از تمام ویژگی های مطالعه شده طبقه بندی واکنش های شیمیایی مشخص کنید.
2. واکنش ثبت شده را از نظر فرآیندهای اکسیداسیون- احیا در نظر بگیرید.
3. خواص فیزیکی هیدروژن را که به طور مستقیم در طول آزمایش مشاهده شده است، توصیف کنید.
4. توضیح دهید که چگونه هیدروژن را می توان تشخیص داد.
آزمایش 2. به دست آوردن، جمع آوری و شناخت آمونیاک
دستگاه را همانطور که در شکل 113 نشان داده شده است مونتاژ کرده و نشتی را بررسی کنید.
یک قاشق غذاخوری کلرید آمونیوم و هیدروکسید کلسیم را در یک فنجان چینی بریزید تا مواد بسوزد. مخلوط را با میله شیشه ای هم بزنید و در لوله آزمایش خشک بریزید. آن را با درپوش ببندید و در پایه سه پایه محکم کنید (به شیب لوله آزمایش نسبت به سوراخ توجه کنید!). یک لوله خشک جمع آوری آمونیاک را روی لوله خروجی گاز قرار دهید.
ابتدا لوله آزمایش را با مخلوطی از کلرید آمونیوم و هیدروکسید کلسیم (2-3 ضربه شعله) و سپس در محلی که مخلوط قرار دارد گرم کنید.
برای تشخیص آمونیاک، یک کاغذ فنل فتالئین مرطوب را در نزدیکی دهانه یک لوله آزمایش وارونه قرار دهید.
حرارت دادن مخلوط را متوقف کنید. لوله آزمایشی که آمونیاک در آن جمع آوری شده است را از لوله خروجی گاز خارج کنید. بلافاصله انتهای لوله خروجی گاز را با یک تکه پنبه مرطوب بپوشانید.
بلافاصله دهانه لوله آزمایش برداشته شده را با انگشت شست خود ببندید و آن را در ظرفی حاوی آب فرو ببرید. انگشت خود را فقط زیر آب بردارید. چه چیزی را مشاهده می کنید؟ چرا آب در لوله آزمایش بالا آمد؟ سوراخ لوله آزمایش زیر آب را با انگشت خود ببندید و آن را از ظرف خارج کنید. 2-3 قطره محلول فنل فتالئین را به لوله آزمایش اضافه کنید. چه چیزی را مشاهده می کنید؟
واکنش مشابهی را بین محلول های قلیایی و نمک آمونیوم هنگام گرم شدن انجام دهید. کاغذ نشانگر مرطوب را روی دهانه لوله آزمایش بمالید. چه چیزی را مشاهده می کنید؟
سوالات و وظایف
1. هنگام واکنش کلرید آمونیوم و هیدروکسید کلسیم چه اتفاقی می افتد؟ معادله ای برای واکنش ایجاد کنید و آن را با استفاده از تمام ویژگی های مطالعه شده طبقه بندی واکنش های شیمیایی مشخص کنید.
2. خواص فیزیکی آمونیاک را که مستقیماً در آزمایش مشاهده می شود، توضیح دهید.
3. حداقل دو راه برای تشخیص آمونیاک را شرح دهید.
گزینه 2.
آزمایش 1. به دست آوردن، جمع آوری و شناخت اکسیژن
دستگاه را همانطور که در شکل 114 نشان داده شده است مونتاژ کرده و نشتی را بررسی کنید. پرمنگنات پتاسیم KMnO را در لوله آزمایش تا حدود ¼ حجم آن بریزید. 4 و یک گلوله پنبه شل را در دهانه لوله آزمایش قرار دهید. لوله آزمایش را با یک درپوش با لوله خروجی گاز ببندید. لوله آزمایش را در پایه سه پایه محکم کنید تا انتهای لوله خروجی گاز تقریباً به انتهای ظرفی که اکسیژن در آن جمع می شود برسد. وجود اکسیژن در رگ را با یک ترکش در حال دود بررسی کنید.
سوالات و وظایف
1. وقتی پرمنگنات پتاسیم گرم می شود چه اتفاقی می افتد؟ معادله ای برای واکنش ایجاد کنید و آن را با استفاده از تمام ویژگی های مطالعه شده طبقه بندی واکنش های شیمیایی مشخص کنید.
2. واکنش ثبت شده را از نظر فرآیندهای اکسیداسیون- احیا در نظر بگیرید.
3. خواص فیزیکی اکسیژن را که مستقیماً در آزمایش مشاهده می شود، توصیف کنید.
4. توضیح دهید که چگونه اکسیژن را تشخیص دادید.
آزمایش 2. به دست آوردن، جمع آوری و شناسایی مونوکسید کربن (IV)
چند تکه گچ یا سنگ مرمر را در یک لوله آزمایش قرار دهید و 1-2 میلی لیتر اسید کلریدریک رقیق اضافه کنید. به سرعت لوله را با یک درپوش و یک لوله خروجی گاز ببندید. انتهای لوله را داخل لوله آزمایش دیگری حاوی 2-3 میلی لیتر آب آهک قرار دهید.
چند دقیقه حباب های گاز از آب آهک عبور می کنند.
سوالات و وظایف
1. وقتی گچ یا سنگ مرمر با اسید کلریدریک واکنش می دهد چه اتفاقی می افتد؟ معادله ای برای واکنش ایجاد کنید و آن را با استفاده از تمام ویژگی های مطالعه شده طبقه بندی واکنش های شیمیایی مشخص کنید.
2. واکنش انجام شده را در پرتو تئوری تفکیک الکترولیتی در نظر بگیرید.
3. خصوصیات فیزیکی مونوکسید کربن (IV) را که مستقیماً در آزمایش مشاهده می شود، توصیف کنید.
4. نحوه شناسایی مونوکسید کربن (IV) را توضیح دهید.
این واکنش نسبت به دی اکسید کربن کیفی است.
درجه 11
کار عملی شماره 1"به دست آوردن، جمع آوری و شناخت گازها"
گزینه 1. دریافت، جمع آوری و شناسایی هیدروژن
دریافت، جمع آوری، شناسایی هیدروژن و انجام آزمایش هایی که ویژگی های آن را مشخص می کند. معادلات واکنش های مربوطه را بنویسید.
مقدار کمی اسید کلریدریک در یک لوله آزمایش ریخته شد و یک گرانول روی در آن ریخته شد. لوله آزمایش با یک درپوش با یک لوله خروجی گاز بسته می شد که انتهای آن به یک لوله آزمایش دیگر وارونه می شد. رها شدن حباب های گاز هیدروژن را مشاهده می کنیم. پس از مدتی، لوله آزمایش دوم را برگرداندند و یک مشعل که با دقت در حال سوختن بود آورده شد. هیدروژن می سوزد و آب بر روی دیواره های لوله آزمایش متراکم می شود.
گزینه 2. دریافت، جمع آوری و تشخیص اکسیژن
دریافت، جمع آوری، شناسایی اکسیژن و انجام آزمایش هایی که خواص شیمیایی آن را تایید می کند. معادلات واکنش های مربوطه را بنویسید.
کمی پرمنگنات پتاسیم داخل لوله آزمایش ریخته و یک گلوله پنبه داخل آن گذاشته و با یک درپوش با لوله خروجی گاز بسته می شود. سپس لوله آزمایش را روی پایه محکم کردند تا انتهای لوله به کف شیشه ای که اکسیژن در آن جمع می شود برسد. لوله آزمایش را گرم کردیم، یک لیوان پر از اکسیژن جمع کردیم (پر بودن لیوان را با ترکش در حال دود بررسی می کنیم، شعله ور می شود) و روی لیوان را با مقوا پوشاندیم.
گزینه 3. دریافت، جمع آوری و شناسایی دی اکسید کربن
دریافت، جمع آوری، شناسایی دی اکسید کربن و انجام آزمایش هایی که خواص شیمیایی آن را تایید می کند. معادلات واکنش های مربوطه را بنویسید.یک تکه زغال سنگ را برداشتند، آن را در شعله مشعل گرم کردند و در ظرفی با اکسیژن فرو کردند، با شعله زرد مایل به آبی آتش گرفت.
گزینه 4. تولید، جمع آوری و شناخت اتیلن
مخلوطی متشکل از یک قسمت استات سدیم بی آب و دو قسمت هیدروکسید سدیم (بی آب) در یک لوله آزمایش مجهز به لوله خروجی گاز قرار داده شد. لوله آزمایش به صورت افقی روی پایه نصب شده و گرم می شود. گاز آزاد شده با برم و محلول پرمنگنات پتاسیم به لوله های آزمایش جداگانه منتقل شد. محلول ها رنگ خود را تغییر نمی دهند. گاز آزاد شده از لوله را آتش زدیم؛ با شعله آبی و غیر درخشان می سوزد. مقدار کمی اسید سولفوریک غلیظ در یک لوله آزمایش قرار داده شد.